Открытие очень долгоживущих белков может объяснить причины старения клетки и возникновения нейродегенеративных заболеваний
Одна из самых больших тайн биологии – почему стареют клетки. Ученые из Института биологических исследований Солка (Salk Institute for Biological Studies), США, нашли «ахиллесову пяту» нейронов головного мозга, вполне вероятно, вносящую решающий вклад в процесс его старения и развитие нейродегенеративных заболеваний.
Исследователи установили, что так называемые очень долгоживущие белки (extremely long-lived proteins, ELLPs), входящие в состав ядерных мембранных каналов нейронов, отличаются чрезвычайно большой продолжительностью существования. В статье, опубликованной в журнале Science, исследователи сообщают, что в мозге крыс им удалось обнаружить ELLPs, возраст которых равен возрасту самого организма. (Для сравнения, продолжительность жизни большинства белков составляет около двух дней.)
Профессор лаборатории молекулярной и клеточной биологии Мартин Хетцер (Martin Hetzer) и его группа первыми открыли важную внутриклеточную молекулярную машину, компонентами которой являются ELLPs, и показали, что в течение всей жизни эти белки не подвергаются замене.
Белки ELLPs составляют транспортные каналы в мембране ядра, так называемые ядерные поровые комплексы (nuclear pore complex, NPC),– ворота, контролирующие поступление и выход в ядро и из ядра различных веществ. Большой «срок службы» этих белков мог бы быть их преимуществом, если бы не происходящий с течением времени износ. В отличие от других белков организма аберрантные химические изменения и другие повреждения, постепенно накапливающиеся в ELLPs, не приводят к их замене.
Накопившиеся в ELLPs повреждения снижают способность состоящих из этих белков трехмерных транспортных каналов защищать ядро клетки от токсинов. Проникающие в ядро токсины могут вызвать изменения в ДНК и, следовательно, в активности генов, способствуя тем самым старению всей клетки.
Многочисленные предыдущие исследования позволяют заключить, что в основе процесса старения лежат изменения в экспрессии генов. Но до открытия лабораторией профессора Хетцера «слабого звена» ядерных поровых комплексов млекопитающих, позволяющего повреждающим ДНК токсинам проникать в ядро, у научного сообщества не было ясного представления о том, чем именно вызываются эти изменения в экспрессии.
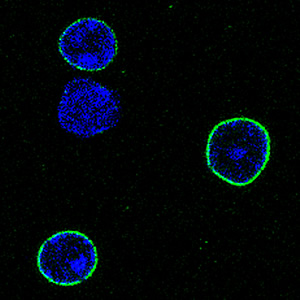
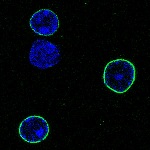
Микрофотография очень долгоживущих белков (extremely long-lived proteins) на поверхности ядра
нейронов головного мозга крысы, светящихся зеленым светом. ДНК внутри ядра показана синим. Ученые из Института Солка доказали, что ELLPs, входящие в состав каналов в ядерной мембране нейронов, существуют более года. Разрушение этих белков позволяет токсинам проникать в ядро, что ведет к старению клетки.
(Brandon Toyama, Salk Institute for Biological Studies)
«Основной определяющей чертой старения является общее снижение функциональных возможностей различных органов, например, сердца и мозга», – объясняет профессор Хетцер. «Это снижение объясняется нарушением гомеостаза, или состояния внутреннего равновесия, клеток, составляющих эти органы. Недавними исследованиями нескольких лабораторий срыв белкового гомеостаза был связан с ослаблением функций клеток».
Полученные профессором Хетцером и его группой результаты предполагают, что ослабление функций нейронов берет свое начало в ELLPs, разрушающихся параллельно с накапливающимися с течением времени повреждениями.
«Большинство клеток, но не нейроны, борются с ослаблением функциональных способностей своих белковых компонентов посредством замены белков, когда их потенциально поврежденные части заменяются новыми функциональными копиями», – продолжает ученый. «Наши результаты дают основания предполагать, что изнашивание ядерных пор может являться общим механизмом старения, приводящим к возрастным дефектам в функции ядра, таким как потеря программы экспрессии генов, характерной для юношеского возраста».
Полученные результаты могут оказать влияние на понимание молекулярных основ старения и таких нейродегенеративных заболеваний, как болезнь Альцгеймера и болезнь Паркинсона. В предыдущих исследованиях профессор Хетцер и его группа обнаружили крупные филаменты в ядрах нейронов старых мышей и крыс, происхождение которых восходит к цитоплазме нервной клетки. Такие филаменты связываются учеными с различными нейродегенеративными заболеваниями, включая болезнь Паркинсона. Являются ли эти аномальные молекулы причиной или результатом заболевания? Ученые пока не пришли к единому мнению. С другой стороны, профессор Хетцер зафиксировал возрастной спад в функционировании ядерных поровых комплексов в нейронах нормально стареющих крыс, являющихся лабораторными моделями биологии человека.
Финансируемая Медицинским фондом Эллисона (Ellison Medical Foundation) и Фондом медицинских исследований Гленна (Glenn Foundation for Medical Research) группа профессора Хетцера – единственная в мире лаборатория, занимающаяся изучением роли транспортных каналов – ядерных поровых комплексов – в процессе старения.
Источник
1752
2012.02.06 13:01:51
