Через 10—20 лет мы все будем ездить на электромобилях

Почему до 2005 года широкое производство электромобилей было невозможным, что сделали нанотехнологии для усовершенствования аккумуляторов и на каких электромобилях мы будем ездить через 10—20 лет, рассказывает заведующий кафедрой электрохимии химфака МГУ, член-корреспондент РАН Евгений Антипов.
Летом 2007 года среди американских студентов провели опрос: их попросили назвать десять главных угроз устойчивому развитию человеческой цивилизации. На первом месте, по их мнению, оказалась проблема иссякания невозобновляемых природных ресурсов. Энергия термоядерного синтеза — это пока далекое будущее, а доступные сейчас возобновляемые источники энергии (ветер, солнце, приливы) дают энергию, во много раз более дорогую, чем природное топливо. Подсчитано, что если покрыть солнечными батареями всю территорию Чада, этой энергии будет достаточно, чтобы покрыть все потребности человечества к 2050 году.
Однако и ветер, и Солнце, и приливы — это источники циклического действия. Поэтому их энергию необходимо накапливать с наименьшими потерями, то есть для этого нужны высокоэффективные аккумуляторы.
С другой стороны, от бензиновых двигателей страдает экология больших городов. Электромобили привлекательнее с точки зрения сохранения здоровья людей:
в Европе уже есть города, куда можно приехать только на электромобиле, но пока это только города для состоятельных людей в Альпах, например известный горнолыжный курорт Церматт в Швейцарии.
Реальность такова, что мы не сможем уйти от использования ископаемых источников энергетического сырья в ближайшее время, поэтому перед нами стоит еще одна задача — использовать энергию как можно более эффективно и экономно. И для достижения этой цели тоже необходимо применять аккумуляторы.
Внедрение электромобилей — возможность принципиально повысить эффективность использования энергии.
Для сравнения: эффективность двигателя самого современного двигателя Audi 4.2 L при мощности в 326 л. с. составляет всего 40%, а эффективность передачи энергии от топливного бака к колесу — 20%. Эффективность мотора электромобиля мощностью 320 л. с. — более 90%, при близкой (90%) эффективности передачи энергии от аккумуляторных батарей к колесу.
Энергоэффективность электромобилей связана и с их экономической привлекательностью при эксплуатации.
Один из коммерчески доступных сейчас электромобилей на литиевых аккумуляторах — Nissan Leaf — по цене на милю пробега обходится в три раза дешевле современных автомобилей с двигателем внутреннего сгорания (учитывая только энергозатраты).
Nissan Leaf с 2010 года продается в США и с прошлого года — в Европе. Его аккумулятор весит 300 кг, мощность — 120 л. с., средний пробег на полной зарядке аккумулятора — 150 км, скорость — до 150 км/ч. От обычной розетки он заряжается семь часов, от специальной станции — тридцать минут. Он оснащен аккумулятором, где в качестве катода используется LiMn2O4.
Сейчас планы большей части автомобильных компаний таковы, что за гибридами первого и второго поколений в 2012—2013 годах большинство серьезных игроков планируют вывести на рынок полноценные электромобили.
Таким образом, нет сомнения, что через 10—20 лет многие из нас будут ездить на электромобилях. Тенденции рынка отражают привлекательность электромобилей.
Перспективы рынка литиевых аккумуляторов выглядят сейчас очень многообещающе: в течение ближайших 10 лет их производство в ценовом исчислении увеличится более чем в пять раз. Эффективность инвестиций в этом секторе будет составлять 22% годовых на период до 2019 года.
«Аккумуляторные технологии — один из самых важных аспектов, определяющих технологическое будущее человечества», — считает Чарли Мунгер, вице-президент компании «Беркшир», которой владеет Уоррен Баффет.
Основной вклад в этот рост отрасли — до 40% к 2019 году (прирост инвестиций — 80% в год) — будут давать электромобили. Остальное — это портативная электроника, крупные накопители энергии и робототехника.
Стоит отметить, что до 2005 года производство электромобилей для широкого использования было невозможным.
Почему же сейчас они стали реальностью? Для этого нужно разобраться, как действовали литиевые аккумуляторы прошлого и как работают современные аккумуляторы.
Аккумуляторная нанореволюция
Чтобы понять это, разберемся с устройством обычного аккумулятора, где в качестве анода используется графит, а в качестве катода — кобальтат лития (см. рисунок ниже). Эти два электрода разделены электролитом, который может проводить только ионы лития, но не обладает электронной проводимостью (перенос электронов происходит только по внешней цепи, которая и служит источником питания для соответствующих устройств).
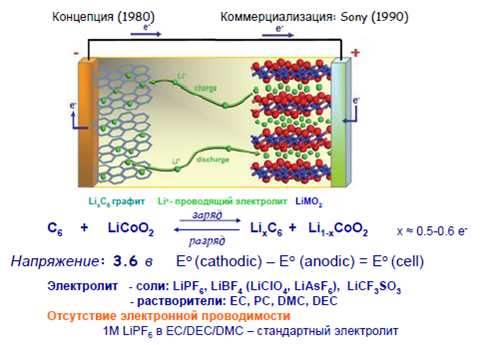
Устройство литий-ионного аккумулятора//Евгений Антипов.
При зарядке аккумулятора ионы лития уходят из соединения LiCoO2, двигаясь через электролит к аноду. Они встраиваются в структуру анода с образованием графитита лития (LiC6). Степень извлечения ионов лития из катода составляет около 50%. Когда мы замыкаем внешнюю цепь, происходит обратный процесс. Ионы лития из анода (восстановителя) переносятся в катод (окислитель), и одновременно во внешней цепи электроны движутся в том же направлении (так достигается общая электронейтральность процесса), и создается электрический ток. В этом случае разность потенциалов двух электродов составляет примерно 3,6 В.
Главная характеристика аккумулятора — количество энергии, которое можно запасти на единицу массы.
Есть два пути повысить эту величину: увеличить разность потенциалов между электродами либо уменьшить молекулярную массу электродов и/или увеличить количество электронов, участвующих в окислительно-восстановительном процессе, на единицу массы электрода.
Впервые предложил использовать LiCoO2 в качестве катодного материала для аккумулятора ученый из США Джон Гуденаф в 1980 году.
Почему таким успехом пользуются именно аккумуляторы на литии?
Одна из причин такой популярности — электролит. Необходимо, чтобы электролит аккумулятора был устойчив при рабочей разности потенциалов. Именно поэтому для этого не подходит вода: для нее «окно электролита» — всего 1,23 В. При превышении этого значения происходит либо ее окисление с выделением кислорода, либо восстановление с выделением водорода, то есть практически невозможно уйти за 2 В.
Органические Li-электролиты выдерживают разницу потенциалов до 4 В, твердые электролиты — до 10 В.
Если при работе аккумулятора электролит будет окисляться, может произойти взрыв.
Именно поэтому электроды должны работать в области стабильности данного конкретного электролита, и для лития такой электролит (растворы солей лития в органических апротонных растворителях) был найден. Кроме этого, от электролита требуется высокая электропроводность по ионам лития — это позволяет избежать потерь энергии. И самое важное — ион лития по размеру маленький, поэтому он легко перемещается, высвобождаясь из одной кристаллической структуры и встраиваясь в другую. Когда он внедряется или извлекается, не происходит больших объемных изменений. Это можно сравнить с тем, как маленькая собачка выбегает из конуры и вбегает в нее — конура остается целой, а если туда зайдет слон, то конура сломается. Аналогичным образом при высвобождении лития из структуры электродов объемные изменения не превышают 5—10%, а в случае натрия они уже составляют более 20%. Поэтому натриевые электроды будут разрушаться, трескаться, механически ломаться. Еще один плюс лития — это однозарядный катион, и он образует относительно слабые связи. Небольшой по размеру и недорогой алюминий был бы перспективен, но это трехзарядный катион, то есть образует намного более прочные химические связи и не может легко высвобождаться.
Теперь переходим ко второму компоненту катодного материала — кобальту. В состав катода должен входить переходный металл, который может окисляться при извлечении иона лития из структуры для сохранения электронейтральности. И это должен быть легкий металл (к счастью, легкие металлы, как правило, самые дешевые), а сам катод должен характеризоваться высокой электронной проводимостью. Кроме того, для работы аккумулятора нужен быстрый транспорт ионов лития, иначе мы не сможем быстро заряжать и разряжать его, то есть не сможем достичь нужных мощностных характеристик.
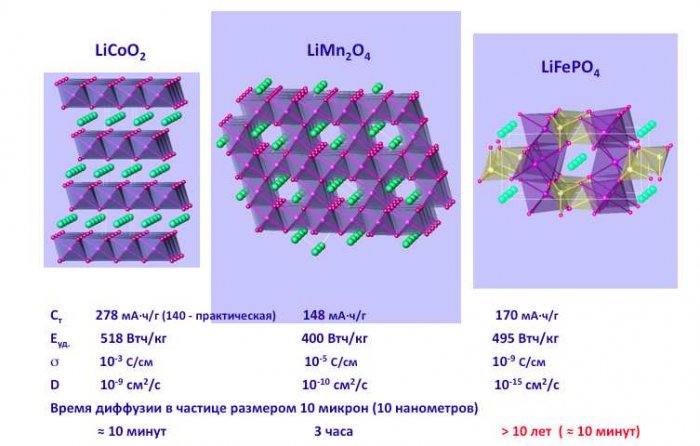
Основные типы литий-ионных аккумуляторов.
Сегодня используются три основных материала для катодов.
LiCoO2 есть в кармане каждого из нас — в мобильном телефоне. LiMn2O4 — это катодный материал аккумуляторов первого электромобиля — Nissan Leaf.
Материал на основе LiFePO4 со структурой оливина был открыт в качестве катода литий-ионного аккумулятора 15 лет назад и сейчас считается самым перспективным материалом, который в будущем совершит электромобильную революцию.
Среди тройки «кобальт, никель, железо» кобальт — самый дорогой, его распространенность в земной коре — наименьшая, он ядовитый и экологически вредный. Кроме того, у аккумуляторов на основе LiCoO2 есть верхний предел по допустимой емкости: до 50% ионов лития можно извлекать из структуры соединения. Если из него извлечь весь литий, структура становится нестабильной. Кобальт переходит в степень окисления +4 и может окислять кислород, выделяющийся атомарный кислород окисляет электролит, и происходит взрыв. Поэтому ни в коем случае нельзя покупать такие аккумуляторы с декларируемой повышенной емкостью, потому что это вещество с малым содержанием лития (менее 50%) крайне взрывоопасное. Этот риск есть, даже когда мы извлекаем небольшое количество лития. Если в структуре имеются какие-либо дефекты, извлечение будет неравномерным, и при извлечении всего лития из одного слоя в структуре может произойти катастрофически быстрое разрушение аккумулятора. Именно поэтому аккумуляторы, подобные аккумуляторам в мобильных телефонах, нельзя использовать в больших устройствах и они не могут работать в электромобилях.
Поэтому для более мощных устройств были начаты поиски другого катодного материала, и в 1997 году Джон Гуденаф предложил использовать LiFePO4. Он дешевый — этот минерал (трифилит) есть в земной коре и не создает никаких экологических проблем. Но у него очень плохая электронная проводимость, то есть это изолятор. Кроме того, у него очень низкий коэффициент диффузии ионов лития: для извлечения этих ионов из структуры соединения при зарядке аккумулятора требуется очень большое время в случае использования частиц катодного материала размером более микрона.
Еще в 2002 году в авторитетнейшем научном журнале Nature опубликовали статью, где утверждалось, что этот материал не имеет никакого будущего с точки зрения промышленного использования.
Тем не менее он безопасен и с точки зрения взрывоопасности: из него не может выделиться кислород, так как он весь очень прочно связан фосфором с образованием устойчивого фосфат-иона.
Решение пришло со стороны новой сферы науки — нанотехнологий.
Если этот материал раздробить на очень маленькие частички, то это критически уменьшит необходимое время извлечения лития. Частички сделали пластинчатыми с малыми размерами вдоль направления движения ионов лития и покрыли нанометровым слоем углерода (теперь это уже наноструктурированные композитные материалы). Этот механизм модификации был предложен в 2005—2007 годах в Массачусетском технологическом институте (МИТ).
Это позволило чрезвычайно быстро извлекать литий из LiFePO4, сохранив его преимущества с точки зрения экологии и безопасности. Сейчас идут активные патентные войны за правообладание этой технологией.
Такие наночастицы LiFePO4 можно заряжать за 10 минут, а если модифицировать покрытие — и за 1—3 минуты. Материал очень устойчивый, и электромобиль на нем сможет работать до 10 лет. Уже сейчас реализован цикл зарядки-разрядки в течение 5—10 минут — и это на совершенно безопасном материале.
Подводя итог, можно сказать, что с точки зрения науки проблемы того, чтобы быстро запасать (или использовать) много энергии, причем дешево и безопасно, в той или иной мере решены. Сейчас слово за широким технологическим внедрением этих разработок, которые позволят электромобилям стать основным видом транспорта в городах в ближайшем будущем.
Источник
2981
2012.07.30 13:01:47