Органическая химия и органический синтез

Органическим синтезом называется получение более сложных органических веществ из менее сложных органических или неорганических веществ. Путём органического синтеза из угля можно получить мыло и уксус, из дерева — шёлк и шерсть, из спирта — каучук. В настоящее время мы широко пользуемся предметами, материал которых изготовляется с помощью органического синтеза. Это — платье, обувь, детали машин, игрушки, лекарства, краски, посуда, женские сумки, пуговицы и многое, многое другое.
Органический синтез — яркий пример великого значения науки, пример того, как человек, вооружённый знанием, подчиняет себе природу, заставляет её служить своим интересам.
Чудесный элемент
Все окружающие нас тела — земля, люди, животные и растения — состоят из химических элементов. Соединяясь друг с другом в различных комбинациях, эти элементы дают большое число разнообразных химических соединений. Среди ста известных химических элементов особое место занимает углерод. Большинство химиков занимается исследованием соединений углерода. Это не случайно. Углерод входит в состав многих химических соединений. Число известных в настоящее время соединений углерода, так называемых органических, уже превысило 3 миллиона и продолжает быстро возрастать (на данный момент их известно более 27 млн. -прим. ред.). Химики сейчас ежемесячно получают более двух тысяч новых соединений углерода. Химических же соединений, в которые не входит углерод, — неорганических — известно гораздо меньше — менее 100 тысяч.
Быстрое развитие химии углерода или, как её обычно называют, органической химии, связано также с тем, что соединения углерода играют особо важную роль в жизни человеческого организма. Атомы углерода легко соединяются друг с другом и с другими элементами; в результате этого могут образовываться чрезвычайно сложные молекулы с очень большим количеством атомов. Эти сложные молекулы, содержащие углерод, составляют основу всех животных и растительных организмов на Земле. Несомненно, что эти молекулы являются основой жизненных процессов и за пределами нашей планеты. Известно, что вселенная состоит из тех же элементов, что и Земля; известно далее, что основой любых жизненных процессов могут быть только очень сложные химические соединения; известно, наконец, что только один углерод может давать очень сложные молекулы. Таким образом, основой жизни, независимо от того, где она находится, могут быть только соединения углерода.
Органическая химия
Органическая химия как наука возникла более ста лет назад. Впервые начал говорить об органических веществах и органической химии шведский химик Берцелиус. Изучая вещества, содержащиеся в растительных и животных организмах, он убедился, что исследовать эти вещества значительно труднее, чем изучать вещества, получаемые из различных минералов и других неживых тел природы. Эти трудности и заставили Берцелиуса выделить изучение органических веществ в особую отрасль химии.
Однако Берцелиус ошибочно считал, что органические вещества принципиально отличаются от минеральных. В своём учебнике химии, вышедшем в 1827 году, он писал, что «...в живой природе элементы повинуются иным законам, чем в безжизненной», что органические вещества не могут образоваться под влиянием обычных физических и химических сил. Поэтому органическую химию Берцелиус определял как «химию растительных и животных веществ, или веществ, образующихся под влиянием жизненной силы».
Такой взгляд Берцелиуса и его последователей — виталистов {от латинского слова «вита» — жизнь) на происхождение органических веществ был глубоко неверным, идеалистическим. Всё последующее развитие органической химии доказало ошибочность взглядов виталистов.
«Жизненной силы» нет
Уже в 1824 году ученик Берцелиуса Вёлер впервые синтезировал, то-есть получил искусственным путём, органическое вещество — щавелевую кислоту. Щавелевая кислота — вещество растительного происхождения. Она находится в больших количествах в водорослях, грибах, лишайниках, папоротниках. Она придаёт кислый вкус всем известному щавелю. Вёлер получил щавелевую кислоту, нагревая неорганический газ дициан с водой. Эта работа Вёлера долгое время оставалась незамеченной. Более того, сам Вёлер не сумел увидеть её принципиального значения. Четыре года спустя, в 1828 году, Вёлер сделал второе открытие. Он показал, что неорганическое вещество циановокислый аммоний легко можно превратить в продукт жизнедеятельности животного организма — мочевину.
Получение мочевины искусственным путём привлекло широкое внимание научного мира. Однако этот факт ещё не мог поколебать веру в таинственную «жизненную силу». Сторонники «жизненной силы» утверждали, что мочевина, как продукт выделения животного организма, не может считаться настоящим органическим веществом, а находится на грани между органическими и неорганическими соединениями. Если ещё можно приготовить искусственно такие вещества, — говорили они,— то это несомненно нельзя сделать по отношению к более сложным органическим веществам.
Однако развитие науки быстро опровергло эти взгляды. Главную роль здесь сыграли бурные успехи органического синтеза. В 1845 году немецкий химик Кольбе получил искусственным путём уксусную кислоту. Эта кислота — органическое вещество. Образуется она при скисании вина и в виде 3—5%-ного водного раствора употребляется в пищу под названием «уксус». Молекула уксусной кислоты состоит из двух атомов углерода, четырёх атомов водорода и двух атомов кислорода. Кольбе получил уксусную кислоту, взяв в качестве исходных веществ древесный уголь, серу, хлор и воду. После синтеза такого типичного органического вещества, как уксусная кислота, стало ясно, что никакой «жизненной силы» не существует, что процесс образования органических веществ подчиняется обычным физическим и химическим законам.
За сравнительно короткий срок был получен ряд других органических кислот, выделявшихся ранее из растений. Это — винная кислота (встречается в винограде), лимонная (в лимонах, апельсинах), янтарная (в незрелом крыжовнике, винограде), яблочная (в большинстве незрелых плодов) и другие. Постепенно химики научились получать и более сложные органические вещества. Так, в 1854 году, когда было установлено, что жиры представляют собой соединения глицерина с различными органическими кислотами (молекулы которых обычно содержат 16—18 углеродных атомов), был получен искусственным путем жир.
Однако до 60-х годов прошлого столетия синтетические работы химиков носили в значительной степени случайный характер. В своих исследованиях химики-органики действовали неуверенно, наощупь; в теоретических вопросах царил разброд. Отражая общее настроение химиков того времени, Вёлер писал: «Органическая химия может в настоящее время кого угодно свести с ума. Она представляется мне дремучим лесом, полным чудесных вещей, огромной чащей без выхода, без конца, куда не осмеливаешься проникнуть». Теория значительно отставала от практических успехов органической химии. Отставание же теории в свою очередь препятствовало успешной работе в лабораториях.
Создавшееся в органической химии положение хорошо понимал молодой химик, работавший в лаборатории Казанского университета. Этот химик — Александр Михайлович Бутлеров — сыграл в дальнейшем исключительно важную роль в развитии химии.
Структурная теория Бутлерова

Александр Михайлович Бутлеров (1828—1886).
Александр Бутлеров с детских лет увлекался химией, и когда пришло время поступать в университет, он без колебания выбрал естественное отделение философского факультета. В Казанском университете, куда поступил Бутлеров, преподавали выдающиеся учёные, которые горячо любили химию сами и умели увлечь за собой студенческую молодёжь. Огромное влияние оказал на Бутлерова его учитель — знаменитый химик Николай Николаевич Зинин.
Особенно заботливо относился к Бутлерову гениальный русский математик Николай Иванович Лобачевский, бывший в то время попечителем учебного округа. По рекомендации Зинина, Лобачевского и других учёных Бутлеров был оставлен при университете. Защитив магистерскую, а затем и докторскую диссертацию, Бутлеров в 26 лет стал профессором химии. К 30 годам он был одним из самых образованных химиков своего времени. Уже первые работы A. M. Бутлерова затрагивали очень важные вопросы органической химии.
В 1861 году Бутлеров впервые осуществил синтез сахара, действуя на водный раствор формальдегида (применяемого для протравливания семян и известного под названием «формалин») раствором гашёной извести. Сахара — это сложные органические соединения. Даже такой сравнительно простой сахар, как виноградный, называемый глюкозой, содержит в своей молекуле 24 атома. Сахара относятся к важным для питания человека и животных веществам — углеводам. Из этого ясно, какой выдающийся интерес представлял синтез, сахара.
В том же 1861 году A. M. Бутлеров начал блестящие теоретические исследования, прославившие русскую науку. До Бутлерова учёные думали, что установить, как построены молекулы,— невозможно. Такая задача была объявлена неразрешимой. Любые попытки определить взаимное расположение атомш в молекулах считались безнадёжным занятием. Многие учёные, последователи философа-идеалиста Канта, объявили, что строение молекул является непознаваемой «вещью в себе». Считалось поэтому, что химики должны ограничиться только изучением поведения химических веществ во время реакций и не пытаться проникнуть в тайны строения самих молекул. А между тем накопленный в химии большой фактический материал находился в явном противоречии с такими взглядами.
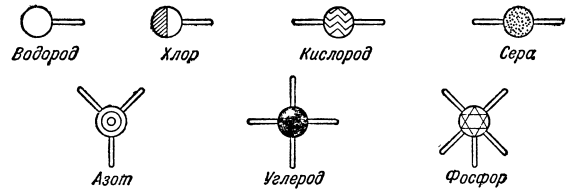
Ещё в 1853 году при исследовании летучих органических соединений металлов было обнаружено, что различные атомы соединяются друг с другом только по определённым законам. Каждый атом одного вещества способен соединяться только с определённым числом атомов другого вещества. Чтобы сравнивать атомы в этом отношении, рассматривают их способность соединяться с атомами водорода. Есть атомы (например, атомы хлора), способные соединяться не более чем с одним атомом водорода. Атомы серы и кислорода соединяются с двумя атомами водорода, азота — с тремя, а углерода — с четырьмя атомами водорода. Водород может всегда соединяться только с одним атомом какого-либо другого элемента.
Способность атома соединяться с определённым числом атомов другого элемента называется валентностью. Атом хлора может соединиться только с одним атомом водорода, и поэтому хлор считается одновалентным; кислород и сера — двухвалентны, азот — трёхвалентен, углерод — четырёхвалентен. Ниже условно изображены атомы наиболее часто встречающихся в органических соединениях элементов с их валентностями.
Глубоко изучив весь этот материал, Бутлеров неопровержимо доказал, что молекулы представляют собой не хаотические скопления атомов, а стройные устойчивые системы, где существует определённый порядок в расположении атомов. В самом деле, молекула воды, например, может быть построена только так, что оба атома водорода соединены с одним атомом кислорода. Никакого другого порядка связи быть не может. Если бы оба атома водорода были прямо связаны друг с другом, то они использовали бы свои валентности полностью и не смогли бы соединиться с кислородом.
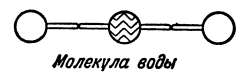
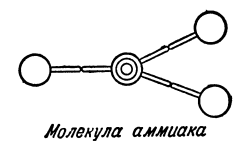
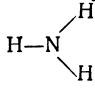
Единственный порядок расположения атомов возможен и для молекулы аммиака, состоящей из одного атома азота и трёх атомов водорода.
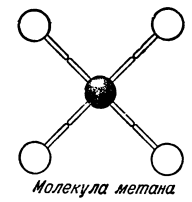
Точно так же обстоит дело и с метаном, или болотным газом, в котором молекула вещества состоит из одного атома углерода и четырёх атомов водорода.
В молекуле углекислого газа на один четырёхвалентный атом углерода приходится два двухвалентных атома кислорода.
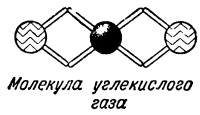
Химики изображают атомы различными буквами латинского алфавита. Вот современное изображение некоторых элементов: водород — H (аш), хлор — Cl (хлор), кислород О (о), сера — S (эс), азот — N (эн, фосфор — P (пэ). Соответственно, молекулы изображаются следующим образом: вода H—О—H (чёрточки между атомами обозначают валентность), аммиак
 , метан
, метан 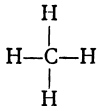 , углекислый газ О = С = О.
, углекислый газ О = С = О. Таким образом, атомы в молекулах расположены в определённом порядке; молекулы обладают определённым химическим строением, которое химик может установить, исследуя вещество. Основную идею своей теории A. M.Бутлеров высказал так: «Исходя из мысли, что каждый химический атом, входящий в состав тела, принимает участие в образовании этого последнего и действует здесь определённым количеством принадлежащей ему химической силы (сродства), я называю химическим строением распределение действия этой силы, вследствие которого химические атомы, посредственно или непосредственно влияя друг на друга, соединяются в химическую частицу».
Установив понятие химического строения, A.M.Бутлеров создаёт новое понятие природы вещества вообще. Он пишет: «Химическая натура сложной частицы (то-есть молекулы) определяется натурой элементарных составных частей (то-есть атомов), количеством их и химическим строением».
Создав понятия химического строения и природы вещества, A.M.Бутлеров вывел органическую химию из теоретического тупика, указал путь к проникновению в глубь молекул, к познанию их внутреннего строения. Он дал основу для понимания химических процессов, для открытия новых путей органического синтеза. Теория Бутлерова сразу же получила боевое крещение, блестяще объяснив ряд вопросов, раньше совершенно непонятных. Следуя за Берцелиусом, химики считали, что свойства вещества могут изменяться только после изменения его состава. Другими словами, если молекула вещества состоит, например, из двух атомов углерода, шести атомов водорода и одного атома кислорода (C2H6O), то никак нельзя ожидать, чтобы нашлось другое вещество, обладающее таким же составом, но другими свойствами.
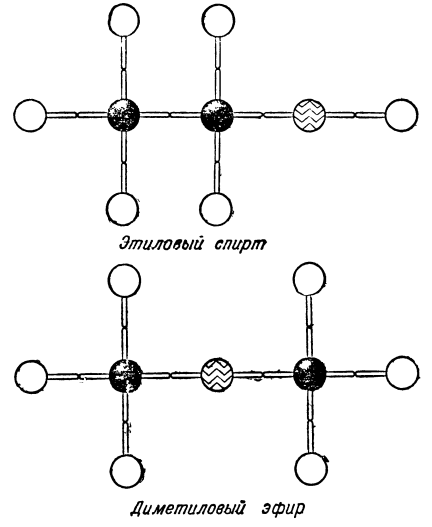
Однако химики открыли два различных вещества с одинаковым составом: C2H6O. Одно из них было давно известно: это — этиловый или винный спирт — жидкость, кипящая при 78,4°. Другое вещество, открытое значительно позднее,— диметиловый эфир — представляет собой газ с приятным эфирным запахом, превращающийся в жидкость при охлаждении его до минус 23,6°. Два совершенно различных вещества имеют одинаковый состав! Как это можно объяснить? Да ведь всё это совершенно ясно,— решил Бутлеров,— что из того, что состав этих веществ один и тот же? Ведь из одинакового количества строительного материала, например, кирпича, досок, железа, стекла, можно выстроить различные здания. Сходным образом природа построила из двух атомов углерода, шести атомов водорода и одного атома кислорода две различные молекулы, расположив в каждой из них «строительный материал» по-разному.
В молекуле спирта кислород связан с углеродом и водородом, а в молекуле эфира — с двумя атомами углерода. Бутлерову стала ясной тайна огромного многообразия органических соединений. Оказывается, дело не только в том, что углерод способен образовывать длинные цепи. Не менее важная причина заключается в возможности различного расположения атомов в молекулах, обладающих одинаковым составом. Честь открытия и объяснения этого замечательного явления, называемого изомерией, принадлежит Бутлерову.
Число изомеров — веществ с одинаковым составом, но разным строением — может быть огромным даже для таких веществ, которые в своём составе имеют только два рода атомов — углерод и водород. Так, для гексана, молекула которого состоит из шести атомов углерода и 14 атомов водорода, возможно пять изомеров; уэйкозана, молекула которого состоит из 20 углеродных и 42 водородных атомов, число возможных изомеров равняется 366 319, а у тетраоконтана (40 углеродов и 82 водорода) может быть 62 491178 805 831 изомер!
Молекулы изомеров отличаются друг от друга внутренним расположением атомов, то-есть своим строением, структурой. Свойства органических веществ в первую очередь определяются строением, структурой молекул. Вот почему Бутлеров назвал свою теорию теорией строения, или структурной теорией.
Могущество теории строения
Теория Бутлерова явилась факелом, который отныне стал освещать путь химиков в их практических исследованиях. Бутлеров первый блестяще доказал силу своей теории на практике. Изучая различные бутиловые спирты, содержащие в молекуле четыре углеродных, 10 водородных и один кислородный атом, Бутлеров обратил внимание на расхождение его теории с практикой. Согласно теории Бутлерова, среди различных спиртов этого состава должен быть спирт, который имеет следующее строение:
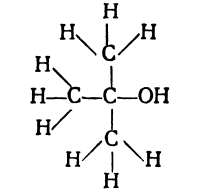
Однако химики такого спирта не знали. И вот Бутлеров, глубоко веря в правильность своей теории, решил получить этот спирт искусственным путём, наметив план синтеза заранее, подобно инженеру, который, прежде чем конструировать машину, составляет ее чертёж. Упорная работа в лаборатории увенчалась успехом: Бутлеров получил этот изомер; впервые в мире на основании научного предвидения было синтезировано вещество неизвестного ранее класса спиртов. Это открытие можно поставить рядом с научным подвигом Д. И. Менделеева, который не только предсказал существование неизвестных химических элементов, но и точно описал свойства этих элементов задолго до их открытия. В дальнейшем Бутлеров, руководствуясь своей теорией, синтезировал целый ряд других спиртов.
Теперь химикам не нужно было блуждать в потёмках и тратить время на огромное число опытов, поставленных наудачу. Стало возможным работать по заранее намеченному плану. Заслуги Бутлерова перед наукой поистине огромны. В 1868 году, рекомендуя A. M. Бутлерова в Петербургский университет, великий химик Д.И. Менделеев писал: «Бутлеров... путём изучения химических превращений стремится проникнуть в самую глубь связей, скрепляющих разнородные элементы в одно целое, принимает за каждой из них врождённую способность вступать в известное число соединений, а различие свойств приписывает различному способу связи элементов. Никто не проводил этих мыслей столь последовательно... A. M. Бутлеров — один из замечательнейших русских учёных. Он русский и по учёному образованию и по оригинальности трудов. Ученик знаменитого нашего академика H. Зинина, он сделался химиком не в чужих краях, а в Казани, где и продолжает развивать самостоятельную химическую школу. Направление учёных трудов A.M. не составляет продолжения или развития идей его предшественников, но принадлежит ему самому. В химии существуют бутлеровская школа, бутлеровское направление».
Со времени создания теории строения Бутлерова прошло более ста лет. Все эти годы химики руководствовались этой теорией и добились огромных успехов. Теория строения нисколько не устарела; сейчас она так же необходима химикам, как и сто лет назад. Характеризуя успехи органической химии, Фридрих Энгельс ещё в 1894 году писал: «Для химии первой половины нашего (XIX) столетия органические соединения были... таинственными вещами. Теперь нам удаётся одно за другим получить их путём синтеза из химических элементов и без помощи органических процессов. Новейшая химия утверждает: как скоро химический состав какого-либо тела известен, оно может быть составлено из элементов. Нам ещё, правда, очень далеко до точного знания состава высших органических соединений, так называемых белковых; однако нет никакого основания сомневаться, что мы, хотя бы спустя столетия, достигнем этого знания и с его помощью будем добывать искусственный белок. Если мы этого достигнем, то вместе с тем мы воспроизведём органическую жизнь, ибо жизнь от самых низших до самых её высших форм есть не что иное, как нормальная форма существования белковых тел».
Глава из книги О.А. Реутова "Органический синтез"
10694
2016.08.01 14:00:29