Новый класс препаратов для лечения рака подавляет активность ферментов необычным способом
Ученые Школы медицины Калифорнийского университета в Сан-Диего (University of California, San Diego School of Medicine) и Онкологического центра Мурса (UC San Diego Moores Cancer Center) нашли новый подход к разработке лекарственных препаратов, позволяющий разрушать раковые опухоли с самой высокой пролиферативной активностью. Это открытие, опубликованное в журнале Nature Medicine, указывает на эффективный альтернативный способ уничтожения быстрорастущих раковых клеток без некоторых отрицательных побочных эффектов, характерных для существующих в настоящее время методов противораковой терапии.
Используя инновационные химические и биологические подходы, ученые во главе с профессором патологии и заместителем директора по трансляционным исследованиям Онкологического центра Мурса Дэвидом Черешем (David Cheresh), PhD, разработали новый класс препаратов, останавливающий деление практически всех раковых клеток путем изменения структуры фермента RAF.
Фермент RAF изучается уже давно, и поэтому для ученых стало полной неожиданностью открытие его роли – жизненно важной для пролиферации клеток и роста опухоли – в клеточном делении.
«Мы открыли эту прежде неизвестную роль RAF в целом ряде опухолей с высокой степенью пролиферации при разработке нового класса препаратов, изменяющих его форму», – говорит профессор Череш.
Существующие сегодня противораковые препараты, мишенями которых являются ферменты, подобные RAF, как правило, рассчитаны на взаимодействие с их активным центром. К сожалению, этим препаратам часто не хватает специфичности. Это означает, что они бьют по разным целям, вызывая нежелательные побочные эффекты, и обладают токсичностью, ограничивающей дозу. Еще хуже то, что опухолевые клетки часто развивают резистентность к препаратам этого класса, снижая их эффективность.
Профессор Череш и его коллеги разработали новый класс ингибиторов RAF, которые не связывают активный центр фермента и таким образом избегают ограничений, свойственных сегодняшним препаратам. Новые препараты, называемые аллостерическими ингибиторами, изменяет форму фермента-мишени и тем самым подавляют его активность. Соединение этого класса, известное как KG5, взаимодействует с RAF только в пролиферирующих клетках, игнорируя покоящиеся. В опухолевых клетках, подвергшихся воздействию такого препарата, RAF не в состоянии взаимодействовать с митотическим аппаратом, обеспечивающим деление клетки. Это ведет к остановке клеточного цикла и апоптозу, или запрограммированной клеточной смерти. Аналогичным образом KG5 эффективно препятствует росту кровеносных сосудов – ангиогенезу.
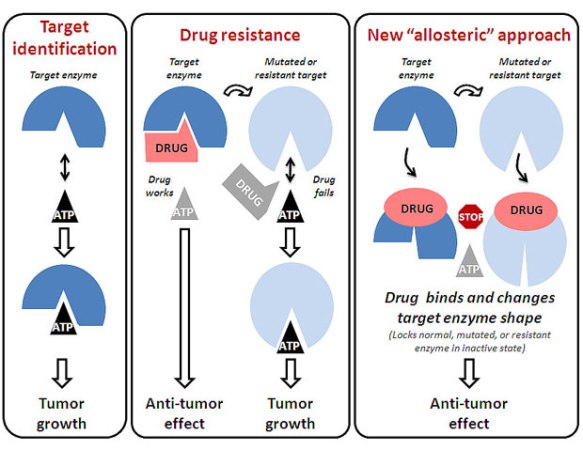
Существующие сегодня противораковые препараты, мишенями которых являются ферменты, подобные RAF-киназам, как правило, рассчитаны на
взаимодействие с их активным центром. Связывание молекулы АТФ с активным центром фермента-мишени стимулирует пролиферацию клеток и дальнейший рост опухоли.
Лекарственный препарат, конкурирующий с АТФ за активный центр фермента, оказывает терапевтическое воздействие, только если фермент-мишень не претерпел конформационных
изменений. В случае мутации или развития резистентности с активным центром взаимодействует молекула АТФ, возвращая развитие событий к первому варианту.
Препараты нового класса не конкурируют с АТФ за активный центр. Они связываются с ферментом и изменяют его форму. В этом случае молекула АТФ лишается доступа к активному центру.
Аллостерические ингибиторы «запирают» нормальный, мутировавший или резистентный фермент в неактивном состоянии. В опухолевых клетках, подвергшихся воздействию такого ингибитора,
неактивный фермент не в состоянии взаимодействовать с митотическим аппаратом клетки, обеспечивающим ее деление, что ведет к остановке клеточного цикла и апоптозу.
(Рис. ucsdnews.ucsd.edu)
«Это необычное открытие, бросающее вызов существующей догме», – считает профессор Череш. «До разработки этого препарата мы понятия не имели, что RAF может способствовать опухолевой прогрессии. И это только один пример того, как при разработке препаратов, избегающих взаимодействия с активным центром фермента, можно найти новые и неожиданные способы нарушения роста опухолей. По сути, мы атакуем важный фермент совершенно по-новому и, тем самым, открываем новые функции, для выполнения которых он предназначен».
KG5 продемонстрировал аналогичные результаты в тестах на линиях раковых клеток, на животных моделях и на биопсийных образцах, взятых у онкологических больных. К настоящему времени ученые разработали варианты KG5 в 100 раз более эффективные, чем первоначальное соединение. Они надеются, что клинические испытания одного из этих более мощных препаратов начнутся в Онкологическом центре Мурса уже в ближайшее время.
Аннотация к статье: A MEK-independent role for CRAF in mitosis and tumor progression
Источник
Используя инновационные химические и биологические подходы, ученые во главе с профессором патологии и заместителем директора по трансляционным исследованиям Онкологического центра Мурса Дэвидом Черешем (David Cheresh), PhD, разработали новый класс препаратов, останавливающий деление практически всех раковых клеток путем изменения структуры фермента RAF.
Фермент RAF изучается уже давно, и поэтому для ученых стало полной неожиданностью открытие его роли – жизненно важной для пролиферации клеток и роста опухоли – в клеточном делении.
«Мы открыли эту прежде неизвестную роль RAF в целом ряде опухолей с высокой степенью пролиферации при разработке нового класса препаратов, изменяющих его форму», – говорит профессор Череш.
Существующие сегодня противораковые препараты, мишенями которых являются ферменты, подобные RAF, как правило, рассчитаны на взаимодействие с их активным центром. К сожалению, этим препаратам часто не хватает специфичности. Это означает, что они бьют по разным целям, вызывая нежелательные побочные эффекты, и обладают токсичностью, ограничивающей дозу. Еще хуже то, что опухолевые клетки часто развивают резистентность к препаратам этого класса, снижая их эффективность.
Профессор Череш и его коллеги разработали новый класс ингибиторов RAF, которые не связывают активный центр фермента и таким образом избегают ограничений, свойственных сегодняшним препаратам. Новые препараты, называемые аллостерическими ингибиторами, изменяет форму фермента-мишени и тем самым подавляют его активность. Соединение этого класса, известное как KG5, взаимодействует с RAF только в пролиферирующих клетках, игнорируя покоящиеся. В опухолевых клетках, подвергшихся воздействию такого препарата, RAF не в состоянии взаимодействовать с митотическим аппаратом, обеспечивающим деление клетки. Это ведет к остановке клеточного цикла и апоптозу, или запрограммированной клеточной смерти. Аналогичным образом KG5 эффективно препятствует росту кровеносных сосудов – ангиогенезу.

Существующие сегодня противораковые препараты, мишенями которых являются ферменты, подобные RAF-киназам, как правило, рассчитаны на
взаимодействие с их активным центром. Связывание молекулы АТФ с активным центром фермента-мишени стимулирует пролиферацию клеток и дальнейший рост опухоли.
Лекарственный препарат, конкурирующий с АТФ за активный центр фермента, оказывает терапевтическое воздействие, только если фермент-мишень не претерпел конформационных
изменений. В случае мутации или развития резистентности с активным центром взаимодействует молекула АТФ, возвращая развитие событий к первому варианту.
Препараты нового класса не конкурируют с АТФ за активный центр. Они связываются с ферментом и изменяют его форму. В этом случае молекула АТФ лишается доступа к активному центру.
Аллостерические ингибиторы «запирают» нормальный, мутировавший или резистентный фермент в неактивном состоянии. В опухолевых клетках, подвергшихся воздействию такого ингибитора,
неактивный фермент не в состоянии взаимодействовать с митотическим аппаратом клетки, обеспечивающим ее деление, что ведет к остановке клеточного цикла и апоптозу.
(Рис. ucsdnews.ucsd.edu)
«Это необычное открытие, бросающее вызов существующей догме», – считает профессор Череш. «До разработки этого препарата мы понятия не имели, что RAF может способствовать опухолевой прогрессии. И это только один пример того, как при разработке препаратов, избегающих взаимодействия с активным центром фермента, можно найти новые и неожиданные способы нарушения роста опухолей. По сути, мы атакуем важный фермент совершенно по-новому и, тем самым, открываем новые функции, для выполнения которых он предназначен».
KG5 продемонстрировал аналогичные результаты в тестах на линиях раковых клеток, на животных моделях и на биопсийных образцах, взятых у онкологических больных. К настоящему времени ученые разработали варианты KG5 в 100 раз более эффективные, чем первоначальное соединение. Они надеются, что клинические испытания одного из этих более мощных препаратов начнутся в Онкологическом центре Мурса уже в ближайшее время.
Аннотация к статье: A MEK-independent role for CRAF in mitosis and tumor progression
Источник
2404
2011.11.29 13:01:38